面對腦癌治療的挑戰


面對腦癌治療的挑戰
腦癌治療面臨了多重挑戰,尤其是較難治癒的多型性膠質母細胞瘤 (GBM)
多型性膠質母細胞瘤 (GBM) 的治療是一項極具挑戰性的任務,主要是由於腫瘤位於腦的深處且受到血腦屏障的保護。這種保護阻礙了化療藥物在腫瘤部位達到有效的濃度。此外,腫瘤邊緣模糊使神經外科醫生難以完全切除。臨床證據顯示,最大程度地切除腦腫瘤 (maximum resection) 對患者的存活期有著極大的幫助。
此外,殘留的腫瘤細胞和腦癌幹細胞可能繼續生長,導致GBM復發率增加。腫瘤切除後,再生微環境進一步增強了殘留腦癌細胞的惡性程度,腫瘤內異質性也限制了單一靶向治療的效果。癌幹細胞、快速增殖和復發均會導致癌細胞惡化。此外,化療藥物的抗藥性和免疫抑制也造成了包括化療和免疫治療在內的常規治療的失敗,加上現行化療藥物常引發神經副作用,增加了家庭照護者的負擔,這些因素都為腦癌患者的預後帶來了極大挑戰。
如果您想進一步了解惡性多型性神經膠母細胞瘤 (GBM) 👉了解更多
GBM的背景
- 無有效治療方式:根據美國癌症協會 (American Cancer Society, ACS)以及美國腦瘤病例登錄中心 (Central brain tumor registry, CBTRUS) 的統計報告顯示,每年估計約有兩萬筆的腦瘤新病人被確診,臺灣每年約有400名惡性膠質腦瘤新病例。醫學上現有治療惡性腦瘤的常規療法,包含手術治療、放射線治療及化學治療,效果非常有限,且因患部受到血腦屏障的保護,目前無真正可治癒藥物,急需新一代療法的開發。
- 快速復發、存活率低:多形性神經膠質母細胞瘤 (Glioblastoma multiformis, GBM) 一個月內最快可長大16倍,是惡化快速的原發性腦瘤,切除後的復發率也非常高,常使病人需要反覆進出醫院接受治療。一般確診為第四期GBM的病人,平均存活時間只有12至18個月。惡性腦瘤擴散程度迅速又難以根除,一旦確診後,通常已是晚期,病人平均存活期往往只有1年左右,5年存活率更只有百分之三點四。現今治療惡性腦瘤的標準治療方針是合併手術、放射治療以及化療,效果都非常有限。
- 多位名人遭逢此不幸:國內外知名的人士因患有GBM無法治癒而死亡,包括美國參議員John Sidney McCain、美國參議員 Edward M. Kennedy、英國政治家 Tessa Jowell、紐約時報記者 Tom Wicker、巴西知名大提琴家Antônio Meneses Neto等,台灣的名人像是前教育部長林清江、作家李敖、龍巖集團創辦人李世聰、政治評論家陳立宏等都是不幸患有GBM後而死亡。
- 診斷:腦瘤的前期最常見到的就是頭痛,臨床症狀會從頭痛、腦壓上升、看到雙重影像、難以說出自己想說的話都是腦瘤的可能症狀,通常是因為腦瘤長大後壓迫到腦組織導致水腫等症狀,所以平時一定要留意身體異狀,若發生以上症狀,且愈來愈嚴重,都有可能是因為GBM的關係,這也是GBM難以早期發現的原因。2018年慈濟醫院就有位郭女士因為暈眩倒地,出現全身突發性癱瘓到院就醫才發現患有GBM。
腦癌治療的挑戰
腦腫瘤位置
- 由頭皮和顱骨保護:除了必須要以手術穿透頭皮與顱骨外,惡性腦腫瘤通常位於即使是最熟練的神經外科醫生也無法觸及的位置。
- 不明確的邊緣 – 難以完全切除腫瘤:腫瘤邊緣模糊使得神經外科醫生難以完全切除,而且可能與生理功能相近的腦區相當的接近,所以要進行到最大程度地切除腦腫瘤成為醫生們的極大挑戰。
血腦屏障 (Blood-brain barrier)
- 血腦屏障 (或稱為血腦障壁) 位於大腦血管系統和中樞神經系統之間,血腦屏障由高度專業化的內皮細胞構成,這些細胞覆蓋著腦毛細血管,並從血管系統和大腦傳遞信號。BBB的結構和功能取決於不同細胞類型(如內皮細胞、星形細胞和外膜細胞)之間的複雜相互作用,以及腦部和血流在毛細血管中的細胞外基質。這些細胞密緊排列,阻止大多數物質進入大腦組織。它的功能是保護大腦免受血液中的毒素、細菌和病毒等有害物質的侵害,同時調節必要分子的運輸並維持穩定的環境。腦、脊髓等中樞神經系統一旦發生疾病時,所使用的藥物大多受BBB的阻擋而無法進入病灶,阻礙了化療藥物在腫瘤部位達到有效的濃度,所以在治療上有非常大的挑戰。
更多關於血腦屏障的內容👉了解更多

腫瘤異質性 (tumor heterogeneity)
- 腫瘤內的異質性指的是個別腫瘤內細胞之間的差異,直接影響預後和治療反應。而腫瘤間的異質性則是在群體層級上觀察到的差異。針對不同的族群給予最有效的治療,將會有助於個人化GBM患者的治療方案。
腫瘤微環境 (tumor microenvironment)
- 癌幹細胞 – 快速增殖和復發:殘留的腦瘤細胞中存在少量的癌幹細胞,這些幹細胞不斷分裂並產生其他不具幹細胞特性的腫瘤細胞,導致腦腫瘤的復發。
- 化療藥物抗藥性:目前的第一線化療藥物Temozolomide長期使用後,神經膠質母細胞瘤會產生O6-甲基鳥嘌呤-DNA甲基轉移酶 (O6-methylguanine methyltransferase, MGMT)。MGMT能修復Temozolomide引起的DNA損傷,使腦瘤對化療藥物產生抗藥性,進而無法有效殺死癌細胞。
- 免疫抑制:腦腫瘤細胞通過調節腫瘤微環境來達到免疫抑制,例如產生多種免疫抑制蛋白,或者抑制抗原呈現細胞並吸引更多的免疫抑制細胞進入腦腫瘤微環境中。這種免疫逃逸現象導致病情惡化速度加快。

生活品質差
- 腦癌治療患者通常面臨手術後的傷口併發症、疼痛、癲癇和水腫,而服用化療藥後也往往引發神經副作用,讓患者的生活品質變差也增加了家庭照護者的負擔。
為何鎖定多型性神經膠母細胞瘤(GBM)
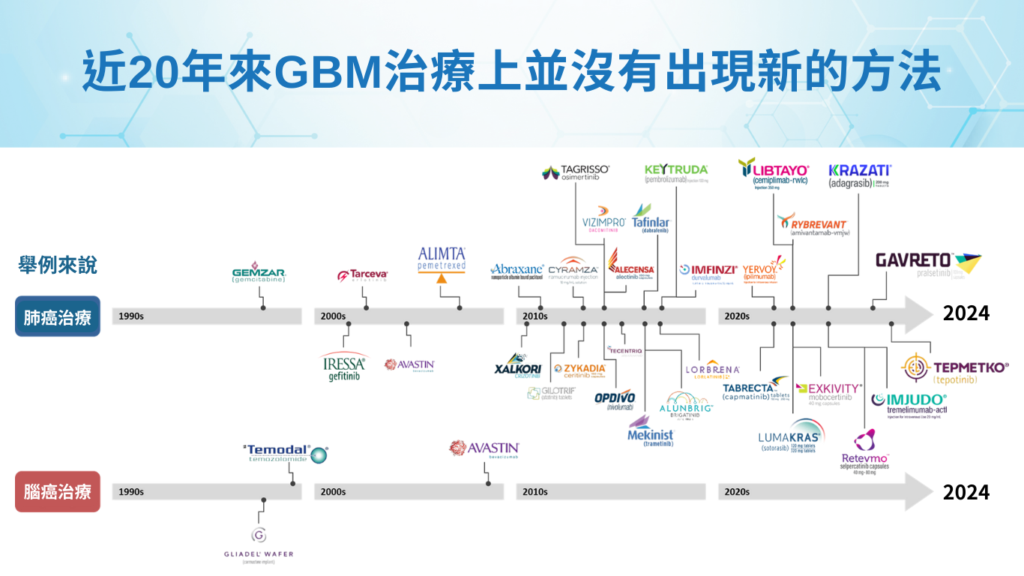
近20年來GBM治療上並沒有出現新的方法,相較於其他癌症治療,如肺癌,近20年來有超過30項藥物上市。
顯示全球在腦癌治療上面臨的困難與挑戰,這也是我們積極切入的主要原因。
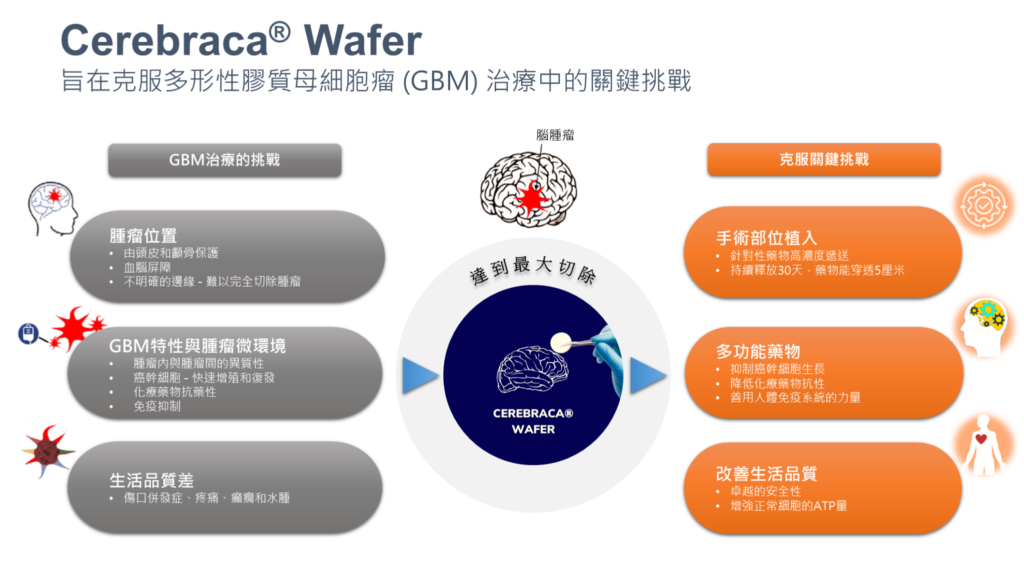
Cerebraca® Wafer旨在克服多形性膠質母細胞瘤 (GBM) 治療中的關鍵挑戰
Cerebraca® wafer的設計就是為了克服治療膠質母細胞瘤的關鍵挑戰,為此優越的臨床結果提供了堅實的基礎。
Cerebraca® wafer的一個關鍵方向是,在腦部手術後它能根除剩餘的腫瘤細胞並抑制癌症幹細胞。Cerebraca® wafer植入手術切除部位,以創建局部的高濃度藥物環境,有良好的穿透力,並且能持續30日釋放藥物,以抑制殘留的腫瘤細胞生長。
在切除腦腫瘤後,再生微環境進一步增強了殘留GBM細胞的惡性程度。腫瘤內異質性限制了單靶向治療的療效。癌症幹細胞、快速增殖和復發導致癌細胞的進展。而化療藥物抵抗和免疫抑制導致了包括化療和免疫治療在內的常規治療的失敗。為了治療這種多方面的情況,Cerebraca® wafer的活性成分EF-API-001是一種多功能藥物,可以針對癌症幹細胞,減少化療藥物抵抗並激活免疫系統。與目前可用的治療方法不同,這些方法通常導致神經副作用和家庭照護者負擔增加,使用Cerebraca® wafer在臨床試驗的結果顯示該治療不會導致額外的不良事件,從而在治療後改善了生活質量。
更多關於Cerebraca® wafer👉了解更多