長弘生技參加Healthcare+ EXPO Taiwan 2023 台灣醫療科技展
日期:2023/11/09
長弘生物科技將於2023/11/30-12/3參加 Healthcare+ EXPO Taiwan 2023 台灣醫療科技展,這是一場不可錯過的亞太醫療生技盛事,也是國內生醫產業搶進世界盃的實力展現,歡迎您的到訪參觀。
【 Healthcare+ EXPO Taiwan 2023 台灣醫療科技展 】預計於11月30日至12月3日登場的「2023 台灣醫療科技展」也是未演先轟動,規模上看2,500展位,包括醫院、科技業到生技業參展成長都超過120%。生策會表示,目前已有東協七個機構先遣買家團洽詢採購,突顯國內生醫產業已有搶進世界盃實力。
備關注的亞太最大醫療盛事-台灣醫療科技展,去年創下18萬人次參觀,今年在AI、大數據、雲端、超級電腦技術爆發,更帶動國內外熱烈參展,瞄準AI在醫療與大健康應用商機,生策會表示,2023台灣醫療科技展三大主題包括:智慧醫療、精準醫療、全齡健康。規模上看2,500展位,包括醫院、科技業到生技業參展成長都超過120%,不僅醫學中心到齊,還有區域/地區醫院、專科醫院超過70多家醫療機構參與,呈現台灣頂尖醫療技術、臨床應用與創新驗證,提供國內外企業合作與採購商洽機會。
長弘生物科技將於2023/11/30-12/3參加 Healthcare+ EXPO Taiwan 2023 台灣醫療科技展,這是一場不可錯過的亞太醫療生技盛事,也是國內生醫產業搶進世界盃的實力展現。此次獲邀於花蓮慈濟醫學中心共同參展 (N802, 4F),將展出抗腦癌新藥的臨床進展與治療神經退化疾病的研發成果,並於12月2日星期六下午一點舉辦一場由林欣榮院長主講 【專家講座】,講題為「Cerebraca® Wafer邁向國際之路」,期待您的到訪。
資料來源:https://expo.taiwan-healthcare.org/zh/news_detail.php?REFDOCID=0ry0sw2jdgpik0z8
【專家講座】
Cerebraca® Wafer邁向國際之路
主講人:
慈濟醫院 林欣榮 院長
長弘生技 劉人瑋 主任
長弘生技 李沅賸 主任
時間:12/2 (星期六) 13:00 – 13:40
地點:N802, 4F (慈濟醫學中心)
參展資訊:
- 展覽日期
日期:2023/11/30(四) – 12/3(日)
時間:10:00 AM ~ 6:00 PM (最終日展至4:00 PM)
- 展覽地點
台北南港展覽館1館4樓
地址:台北市南港區經貿二路1號4樓 觀看地圖
- 參觀資格申請
STEP 1. 登入/註冊會員。
STEP 2. 確認個人基本資料,即完成登錄手續。
STEP 3. 展期至入口出示『入場憑證QRCode』即可掃描入場!
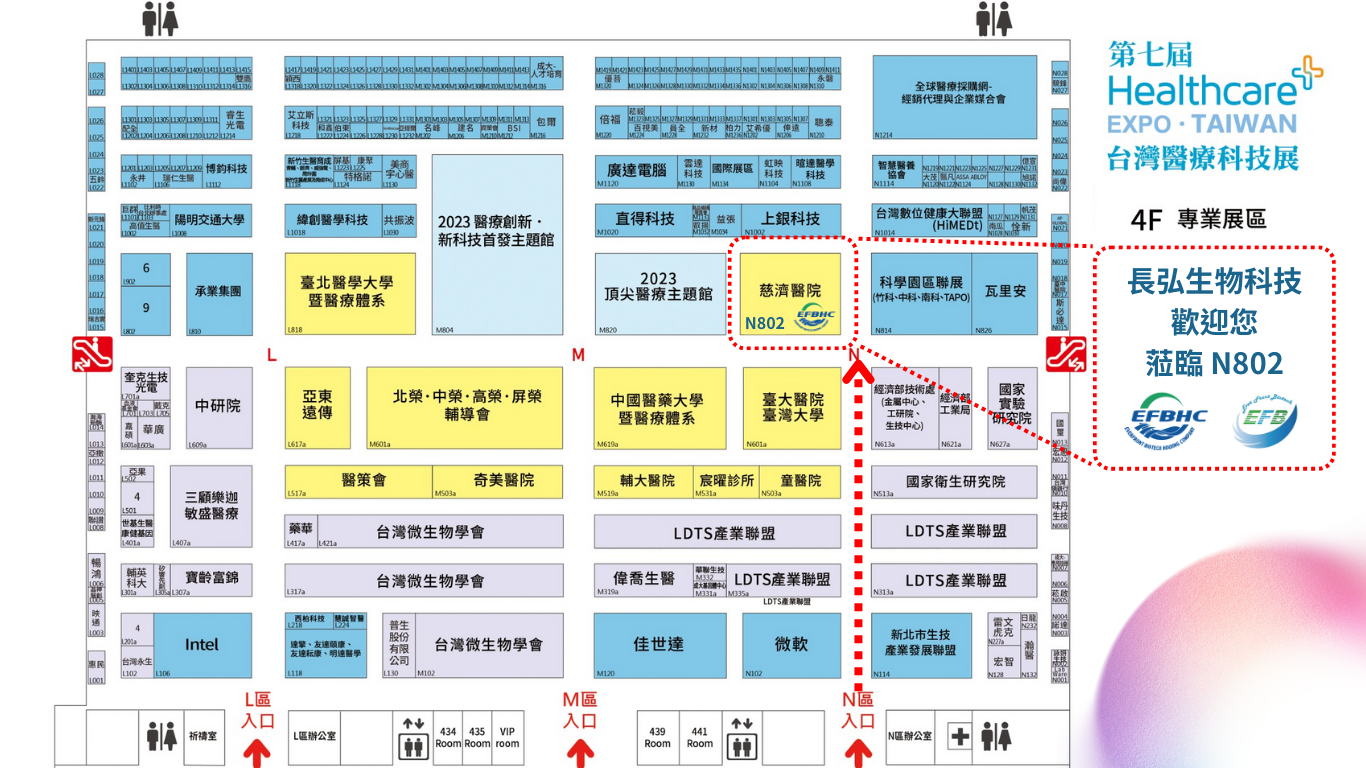
長弘生物科技本次參展攤位位於4F 花蓮慈濟醫學中心 (N802),期待您的來訪。
長弘生物科技控股有限公司 - 腦瘤臨床試驗計畫與新藥研發專案
Cerebraca® Wafer產品亮點:
長弘生物科技以「腦癌治療革命性產品,精準醫療緩釋藥片Cerebraca® Wafer治療惡性腦癌」為主題,透過多項專利新穎性特點,成功開發出此一新藥,成為解決惡性腦癌難以處置且易於復發的問題的新方向。腦癌細胞的高抗藥性讓化療逐漸失效,以及癌幹細胞比例高,進一步導致腦癌復發與難以治療,這些問題都得以被Cerebraca® Wafer的藥物作用機制所解決。此外,惡性腦癌細胞表現PD-L1,會導致體內免疫系統無法毒殺癌細胞,但Cerebraca® Wafer的研發成功,使得此問題也得以改善。在Phase I臨床試驗中,Cerebraca® Wafer展現出卓越的療效,沒有發現與試驗藥物相關的不良反應,復發惡性腦癌患者存活中位數(或平均數)累計已達25-26個月,相較現有策略如格立得植入劑Gliadel® wafer (6.4個月)、帝盟多膠囊 (5.8個月)或癌思停注射液 (9.4個月),療效明顯改善。在台灣衛生福利部及花蓮慈濟醫院人體研究倫理委員會的核准下,Cerebraca® Wafer進行了恩慈治療試驗,對於手術無法切除並長於頸椎處的惡性腦癌患者,僅切開傷口植入Cerebraca® Wafer便使腫瘤縮小。另外,使用Cerebraca® Wafer合併細胞因子誘導的殺手細胞(CIK)進行治療,能達到超過40個月的無復發存活期。Cerebraca® Wafer展現出卓越的臨床成果,長弘生物科技股份有限公司現正積極尋求合作夥伴,共同開發此一新藥,以救助更多惡性腦癌患者。
長弘生物科技股份有限公司簡介:
長弘生物科技成立於2010年,定位在於新藥的研究與發展,著眼於潛力小分子之篩選,並且進一步開發成為商品進入臨床測試。從前端的潛力產品開發,到臨床前研究、化學製造與管制 (CMC)、新藥臨床試驗送審、臨床試驗規劃與執行等項目皆由公司團隊主導。目前長弘生技團隊已有三項臨床試驗驗 (Cerebraca® Wafer, 適應症為惡性腦瘤;HK-001, 適應症為漸凍症;EF-009, 適應症為胰臟癌),申請獲得美國與台灣核准執行臨床試驗。
長弘生物科技新藥開發亦配合國家政策,Cerebraca® Wafer以及HK-001兩項產品於2016年度獲得生技新藥認證。並積極參與國家型計劃之申請,截至2022年度,共有三項科專計畫(業界開發產業技術計畫、A+企業創新研發淬鍊計畫-前瞻技術研發計畫以及A+企業創新研發淬鍊計畫-快速審查臨床試驗計畫 (Fast track) 與一項SBIR計畫獲得經濟部專案補助。